2023年1月18日,成都第一制药有限公司氨甲环酸注射液(规格:5ml:0.5g、5ml:0.25g)仿制药质量与疗效一致性评价获批。(编号:2023B00254、2023B00255)。
氨甲环酸注射液一致性评价研究过程结合日本、德国参比制剂剖析情况,对原辅料包材进行严苛筛选,对工艺参数进行优化,提高了药品质量控制手段。成一制药研究院协同公司生产质量技术中心,以高标准、高规范要求注册研究、注册生产过程。审批过程虽受2022年疫情不可抗力的影响,但技术审评联同研制、生产注册现场核查用时仍提前行业常规用时6个月。
产品提高了药用原辅料和包装材料质量,深入研究了终端灭菌及质量控制等关键技术,达到了原研药品质量一致的标准,并进一步提升了企业工业制造水平和管理水平。至此公司投资3000万的小容量终端灭菌生产线将正式亮相,为未来小容量注射液终端灭菌产品的生产供应打下坚实基础。
以此为契机,公司将以过硬的生产质量为该产品上市保驾护航,并推动公司品种资源的全面盘活和产能释放,为仿制药市场布局打开新局面,开启新篇章。同时,成一制药将积极响应国家政策号召,继续选取临床必须品种,持续推进化学药品仿制药一致性评价,进一步满足人民群众用药需求。
“氨甲环酸TIPS”
近年来中国公立医疗机构终端氨甲环酸注射剂销售情况(单位:万元)
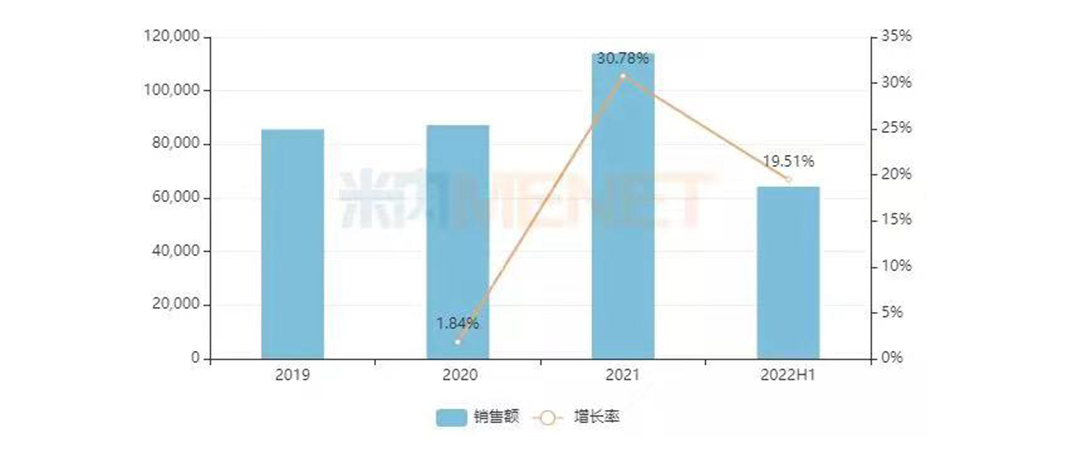
来源:米内网中国公立医疗机构药品终端竞争格局
氨甲环酸注射液属于国家基药、医保甲类品种。其为人工合成的赖氨酸衍生物,属于抗纤维蛋白溶酶药,临床上常被用于治疗急性或慢性、局限性或全身性原发性纤维蛋白溶解亢进所致的各种出血,是经典止血药之一。2021年氨甲环酸注射液在全国公立医疗机构销售额达12亿元,2022年销量继续上涨,预测将达到14亿元。
氨甲环酸注射液已被列入国家第八批集中带量采购名单,目前已启动医疗机构报量工作,2月份将完成报量,预计将在3月份开展企业申报和报价工作。目前该品种已过评企业数已达15家,获得集采入场券,竞争将会异常激烈。而一旦集采中选,无疑将会为产品销售提供更广阔的市场前景。